| Фосфін | |
|---|---|
 |
 |
| Назва за IUPAC | Фосфан |
| Інші назви | Гідрид фосфору, фосфор тригідрид |
| Ідентифікатори | |
| Номер CAS | 7803-51-2 |
| Номер EINECS |
232-260-8 |
| ChEBI |
30278 |
| RTECS |
SY7525000 |
| SMILES |
P[1] |
| InChI |
InChI=1S/H3P/h1H3 |
| Номер Бельштейна |
3600171 |
| Номер Гмеліна |
287 |
| Властивості | |
| Молекулярна формула | PH3 |
| Молекулярна маса | 33,998 г/моль |
| Зовнішній вигляд | безбарвний газ |
| Запах | гнила риба, часник |
| Густина | 1,390 г/л[2] |
| Тпл | -133,8 °C[2] |
| Ткип | -87,75 °C[2] |
| Розчинність (вода) | малорозчинний |
| Розчинність (етанол) | розчинний |
| Розчинність (етери) | розчинний |
| Пов'язані речовини | |
| Пов'язані речовини | дифосфін |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
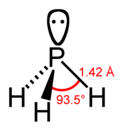
Фосфі́н — неорганічна сполука складу PH3, безбарвний газ із різким запахом гнилої риби. Проявляє слабкі осно́вні властивості, аналогічно до аміаку може утворювати солі — малостійкі сполуки фосфонію.
Фосфін є токсичною речовиною та використовується, як хімічна зброя (військове позначення PH).
Отримання
Основним методом отримання фосфіну є взаємодія сильних лугів чи води із солями фосфонію:
Фосфін можна синтезувати дією хлоридної кислоти на фосфіди активних металів, наприклад, фосфід магнію чи фосфід кальцію:
В результаті цієї реакції може також утворюватися незначна кількість дифосфіну P2H4, який здатен самозайматися. Позбутися побічного продукту можна шляхом його конденсації при охолодженні з льодом.
Хімічні властивості
Фосфін є легкозаймистою сполукою (температура займання 150 °C), процес горіння проходить за рівнянням:
В результаті повного згоряння може утворюватися фосфатна кислота:
Аналогічно до аміаку, при взаємодії з сильними кислотами (наприклад, хлоридною чи хлоратною), утворює солі фосфонію, де виступає катіоном:
Є сильним відновником, відновлює значну кількість металів з водного розчину їхніх солей.
Токсичність
Фосфін належить до речовин загальноотруйної дії, може використовуватися як хімічна зброя. Його токсична дія проявляється при потраплянні до організму — шляхом інгаляції або через стравохід у вигляді сполуки-супутника фосфідів (можуть використовуватися у складі пестицидів). Симптомами отруєння є нудота, болі в животі, утруднене дихання, озноб, спрага, головний біль. За ними можуть слідувати конвульсії або кома[3].
Біосигнатура
Фосфін вважають речовиною, що може бути індикатором життя на планеті. Він існує на Землі лише завдяки біологічним процесам (певні мікроби в безкисневому середовищі можуть його генерувати) або в промислових процесах, де його виробляють люди. У астрономічній спільноті немає інших відомих джерел фосфіну, за винятком умов дуже екстремальних температур, таких як у гарячій щільній внутрішній атмосфері Юпітера та Сатурна (де видно фосфін) або зірок. Створений фосфін руйнується з часом різними процесами, наприклад, реакціями з киснем і воднем або ультрафіолетовими радіаційними реакціями. Це означає, що без джерела, що виробляє фосфін, він повинен повільно зникати з часом.
У 2020 році фосфін начебто був виявлений в атмосфері Венери, що могло бути доказом існування мікробного життя на Венері, які літають у “придатній для життя зоні” атмосфери[4]. Проте, пізніше виявлення фосфіну на Венері спростували ряд дослідників, включаючи фахівців NASA[5].
Див. також
Примітки
- ↑ PHOSPHINE
- ↑ а б в За тиску 101,3 кПа
- ↑ WHO (Data Sheets on Pesticides-No. 46): Phosphine. Inchem.org. Архів оригіналу за 18 лютого 2010. Процитовано 7 серпня 2014. [Архівовано 2010-02-18 у Wayback Machine.]
- ↑ Mason, James (13 вересня 2020). Phosphine in the atmosphere of Venus — what does it mean?. Medium (англ.). Архів оригіналу за 23 вересня 2020. Процитовано 14 вересня 2020.
- ↑ Перший політ на Венеру може відбутися у 2025 році. 07.06.2023, 10:21 pm
Джерела
- CRC Handbook of Chemistry and Physics / D. R. Lide. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5. (англ.)
- Реми Г. Курс неорганической химии / А. В. Новоселова. — М. : ИИЛ, 1963. — Т. 1. — 922 с. (рос.)
- Фосфор // Химическая энциклопедия : в 5 т. / гл. ред. Н. С. Зефиров. — М. : Большая Рос. энцикл., 1998. — Т. 5 : Триптофан — Ятрохимия. — Стб. 282. — Библиогр. в конце ст. — ISBN 5-85270-310-9.(рос.)









![{\displaystyle \mathrm {[PH_{4}]^{+}+OH^{-}\rightarrow PH_{3}+H_{2}O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/275a8ce792fd364d7100ce6305392a92d2297831)



![{\displaystyle \mathrm {PH_{3}+H^{+}\rightarrow [PH_{4}]^{+}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/817ffd09d30f30b292b501ede9d3ccf1dfd2cf80)



