Зауважте, Вікіпедія не дає медичних порад! Якщо у вас виникли проблеми зі здоров'ям — зверніться до лікаря. |

| |
| Систематична назва (IUPAC) | |
| 1-[4-(3-Hydroxyphenyl)-1-methyl-4-piperidyl]propan-1-one | |
| Ідентифікатори | |
| Номер CAS | |
| Код ATC | |
| PubChem | |
| DrugBank | |
| Хімічні дані | |
| Формула | C15H21NO2 |
| Мол. маса | 247,338 г/моль |
| SMILES | & |
| Фармакокінетичні дані | |
| Біодоступність | 34-40% (перорально), 44% (ректально) |
| Метаболізм | ? |
| Період напіврозпаду | 2-4 год. |
| Виділення | ? |
| Терапевтичні застереження | |
| Кат. вагітності |
? |
| Лег. статус | |
| Шляхи введення | перорально, ректально, в/в |
Кетобемідон (англ. Ketobemidone, торгова назва «Кетоган» — синтетичний опіоїдний анальгетик. Його знеболювальна активність знаходиться на рівні морфіну, і він також має деякі властивості антагоніста NMDA-рецептора|, частково завдяки його метаболіту норкетобемідону. Це може зробити його корисним у лікуванні деяких типів болю, які погано реагують на інші опіоїди.[1] Кетобемідон продається в Данії, Ісландії та Норвегії. До 2024 року він був доступний у Швеції, але в цьому році вилучений з аптечного обігу. Кетобемідон застосовується при сильних болях.[2]
Історія
Кетобемідон був вперше синтезований у 1942 році Айслебом та його колегами[3] в лабораторії компанії «IG Farbenindustrie» під час Другої світової війни. Перше дослідження препарату на людях було опубліковано в 1946 році[4], і невдовзі його було введено в клінічну практику. Кетобемідон не використовувався в клінічній практиці в США, тому коли був оприлюднений закон про контрольовані речовини 1970 року, його було віднесено до Списку I з ACSCN 9628. Станом на 2013 рік Управління боротьби з наркотиками жодного разу не призначало річної квоти на його виробництво.[5]
Компанія «Pfizer» виробляє кетобемідон під торговими назвами «Кетоган» і «Кеторакс». Він випускається у вигляді таблеток, супозиторіїв і флаконів для ін'єкцій. У деяких країнах представлений препарат з уповільненим вивільненням, який продається під торговою маркою «Кетодур», який містить 10 або 25 мг кетобемідону.
Фармакологія
Експерименти на колишніх наркоманах показали, що кетобемідон викликає значну залежність, і у високих дозах, порівняно з іншими опіоїдами, може збільшити потенціал зловживання у колишніх і діючих опіоїдних наркоманів. Хоча вперше були запропоновані певні зусилля для розробки проекту резолюції, яка закликає уряди припинити виробництво та використання кетобемідону[6], цей результат не узгоджувався з клінічними спостереженнями, а інше дослідження 1958 року не виявило, що кетобемідон спричинює більшу залежність, ніж морфін. Це дослідження помітило, що в той час як для морфіну доза для ейфорії така ж, як і для аналгезії, для кетобемідону анальгетична доза була значно нижчою від дози для ейфорії. Таким чином, навіть порівняно з морфіном, кетобемідон може бути набагато ефективнішим, не викликаючи значної ейфорії, і таким чином під наглядом кваліфікованого клініциста може мати менший ризик виникнення залежності.[7] Кетобемідон переважно використовується в скандинавських країнах, а Данія лідирує за статистикою його використання.[8]
Метаболізм
Кетобемідон переважно метаболізується шляхом кон'югації фенольних гідроксильних груп і N-деметилювання. Лише близько 13—24 % препарату виводиться в незміненому вигляді після внутрішньовенного введення.[9]
Хімія
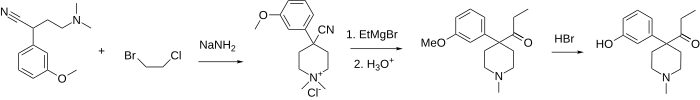
Кетобемідон є 1-метил-4-(3-гідроксифеніл)-4-пропіонілпіперидином. Зазвичай він доступний у вигляді гідрохлориду, який є білим порошком. Кетобемідон синтезується шляхом алкілювання (3-метоксифеніл)ацетонітрилу біс(2-хлоретил)метиламіном, з подальшою реакцією з бромідом етилмагнію, і, нарешті, О-деметилюванням бромистоводневою кислотою.[10]
Через нестабільну природу біс(2-хлоретил)метиламіну розроблено багато інших шляхів отримання кетобемідону. Шлях, зображений нижче, полягає в першому алкілуванні того самого (3-метоксифеніл)ацетонітрилу 2-хлор-N, N-диметилетиламіном або 2-хлор-N-бензил-N-метилетиламіном.[11] Далі ці аміни знову алкілюють за допомогою змішаного 1-бром-2-хлоретану, таким чином завершуючи піперидинове кільце, та отримуючи четвертинну амонієву сіль, яку можна декватернізувати за допомогою тіофенольної солі[12] (для N, N-диметиламонію) або каталітичне гідрування[13] (для обох сполук) до загального 4-(3-метоксифеніл)-4-ціано-1-метил-піперидину. Останній дає кетобемідон після реакції Гріньяра з бромідом етилмагнію та розщеплення ефіру.
Примітки
- ↑ Ebert B, Thorkildsen C, Andersen S, Christrup LL, Hjeds H (вересень 1998). Opioid analgesics as noncompetitive N-methyl-D-aspartate (NMDA) antagonists. Biochemical Pharmacology. 56 (5): 553—9. doi:10.1016/S0006-2952(98)00088-4. PMID 9783723. (англ.)
- ↑ Brayfield A, ред. (9 січня 2017). Ketobemidone Hydrochloride: Martindale: The Complete Drug Reference. MedicinesComplete. London, UK: Pharmaceutical Press. Процитовано 6 вересня 2017. (англ.)
- ↑ GB patent 609763, "Manufacture of piperidyl ketones", published 1948-10-06, assigned to Ciba Ltd.
- ↑ US patent 2486796, Meischer, K.; Kaegi, H., "Esters of 1-alkyl-4-hydroxyphenyl-piperidil-4-ketones" (англ.)
- ↑ DEA Diversion Control Division. Архів оригіналу за 14 травня 2017. Процитовано 3 травня 2014. (англ.)
- ↑ Development of Synthetic Narcotic Drugs. Bulletin on Narcotic Drugs. 1956 (1): 11—14. 1956. Процитовано 5 липня 2012. (англ.)
- ↑ Bondesson, U. (1982). Biological Fate of Ketobemidone in Man. Abstracts of Uppsala Dissertations from the Faculty of Pharmacy. 68. ISBN 978-91-554-1243-2. (англ.)
- ↑ Statistical Information on Narcotic Drugs (PDF). INCB. 2004. Архів оригіналу (PDF) за 7 жовтня 2006. Процитовано 7 вересня 2006. (англ.)
- ↑ Bondesson U, Hartvig P, Danielsson B (1981). Quantitative determination of the urinary excretion of ketobemidone and four of its metabolites after intravenous and oral administration in man. Drug Metabolism and Disposition. 9 (4): 376—80. PMID 6114838. (англ.)
- ↑ William Andrew Publishing (2013). Cetobemidone. Pharmaceutical Manufacturing Encyclopedia. Elsevier. ISBN 9780815518563. (англ.)
- ↑ Avison AW, Morrison AL (1950). 303. Synthetic Analgesics. Part VI. The Synthesis of Ketobemidone. Journal of the Chemical Society (Resumed). 1950: 1469—1471. doi:10.1039/JR9500001469. (англ.)
- ↑ Shamma M, Deno NC, Remar JF (1966). The selective demethylation of quaternary ammonium salts. Tetrahedron Letters. 7 (13): 1375—1379. doi:10.1016/s0040-4039(01)99725-4. (англ.)
- ↑ Kägi H, Miescher K (1949). Über eine neue Synthese morphinähnlich wirkender 4-Phenylpiperidin-4-alkylketone und verwandter Verbindungen. Helvetica Chimica Acta. 32 (7): 2489—2507. doi:10.1002/hlca.19490320736. (нім.)
Посилання
- Ketobemidone. Drug Information Portal. U.S. National Library of Medicine. (англ.)








